- トップ
- このサイトについて
- 理事会報告
- 役員
- 研究会
- 第62回放射線治療技術研究会
- 第61回放射線治療技術研究会
- 第60回放射線治療技術研究会
- 第56回放射線治療技術研究会
- 第55回放射線治療技術研究会
- 第54回岐阜県放射線治療技術研究会
- 第53回岐阜県放射線治療技術研究会
- 第52回岐阜県放射線治療技術研究会
- 第51回岐阜県放射線治療技術研究会
- 第15回岐阜県放射線技師学術大会
- 第49回岐阜県放射線治療技術研究会
- 第48回岐阜県放射線治療技術研究会
- 第47回岐阜県放射線治療技術研究会
- 第46回岐阜県放射線治療技術研究会
- 第45回岐阜県放射線治療技術研究会
- 第44回岐阜県放射線治療技術研究会
- 第43回岐阜県放射線治療技術研究会
- 第42回岐阜県放射線治療技術研究会
- 第41回岐阜県放射線治療技術研究会
- 第40回岐阜県放射線治療技術研究会
Last update 2017/04/28
昭和60年当時岐阜大学医学部放射線科の柳川繁雄先生が、岐阜地区4施設の放射線治療患者を診察していました。そこで、各施設の照射線量の計算方法が異なっていることを疑問に思い、「施設間の標準化を行っては」とのことから、昭和62年7月に岐阜県下の放射線治療に携わる医師、診療放射線技師が年3〜4回集まり情報や技術交流を図る目的で発足誕生しました。
平成5年1月から社団法人岐阜県放射線技師会主催の研究会として会則を整備し再出発をしました。
この研究会は、医師と診療放射線技師が協力して運営してきたため、医師の立場、技師の立場を超えて放射線治療について議論することができ、研究会には岐阜県はもとより、近隣の県から職種を問わず多数の職種が参加できる、開かれた会としています。
岐阜県の各地区より10名の世話人と2名の顧問が選出され、研究会担当理事とともに、研究会開催に当たっては、案内状の作成、送付、司会進行、報告書作成までを協賛メーカーの手を借りず、全て手作りで行っています。
ともすれば、技術偏重になりがちな研究会にあって、放射線治療という特殊な分野ということで、患者様の心のケアも含んだトータルな治療を目指して取り組んでいます。
第53回岐阜県放射線治療技術研究会
| 会員発表1 |
|---|
当院でのMonitor Unit 独立検証法 中津川市民病院 成瀬 徹 会員 |
|
・近年の放射線治療における計画には3次元治療計画装置(RTP)を用いるのが標準である。誤照射防止のため、各施設でMU独立検証が行われているが、その方法や精度は様々であり、施設の判断に委ねられている。当院では平成18年の装置更新時より、全症例にMU独立検証を適用してきたが、その重要さは理解できるものの治療計画時に大きな負担となっている。 (目的) ・臨床現場ではかなり複雑な照射野が用いられる場合も多く、当院では4〜6門以上の多門照射が多い。そこで我々は、従来の検証方法に改良を加えることにより、計算精度の向上、適応範囲の拡大、作業の効率化を成し得たので報告する。 (使用機器) ・リニアック Siemens ONCOR Impression Plus ・RTP Elekta Xio Ver 4.3.1 ・電位計 RAMTEC 1000Plus ・電離箱 PTW30013 Farmer ・ファントム Solid Water RMI 457 ・OS Windows 7 ・開発環境 Visual Studio 2010 (当院における検証方法のまとめ) ・矩形照射野 コリメータ反転効果補正係数(k)を用いて等価正方形のScを算出する。BjarngardとSiddonの式から等価正方形のSpを算出する。 ・単純な不整形照射野 Sc、Spを同一照射野としてそれぞれリーフ開度から自作プログラムにてClarkson積分の放射状距離を 自動計算する。 ・不整形照射野で照射野が体表面からはみ出してしまう場合 Sc、 Spに影響する照射野を分離し、それぞれのリーフ開度から放射状距離を自動計算する。 ・リーフの貫入がある場合 MLC形状と自作スケールによってSpの計算を補正する。 ・線量評価点が軸外にある場合 評価点のパターン別に空中軸外線量比(A0)と実効SWDを算出する。 ・不均質補正がある場合の深さ Xioの実効深の妥当性を目視で評価し深さの値として使用する。実効深の妥当性に疑問があれば、Measure機能を使用しCT断面から肺の長さを計測する。Van Dykの年齢による肺の電子密度換算式を利用することで肺の実効長を算出し計算に使用する。 (結果) ・照射野の形状に応じて検証方法を使い分けることで作業効率が改善した。 ・検証方法の一部をプログラム化したことにより、検証作業の負担が軽減した。 ・複雑な照射野でも正確な検証値が得られるようになった。 ・軸外に線量評価点がある場合でも計算が容易になった。 ・実測による線量評価でもRTP値と比較して遜色ない線量が測定された。 (考察) ・入れ子関数で作成したTPRの回帰式に0.5%程度の誤差があり、まだ改善の余地がある。 ・不均質補正を行う場合の深さの評価には課題を残している。 ・理論上もっとも正確なSc の算出方法は逆投影法であるが、不整型照射野でフラットニングフィルタの逆投影面積を算出するのは難しい。 ・現実的にはRTPが算出したMUで照射せざるを得ないが、そのMUはPerfectではない。 ・正確なMUを計算できる方法を持っていないと、独立検証にはならない。 |
|
| |
当院における前立腺IMRTの現状 岐阜大学医学部附属病院 松山勝哉 会員 |
|
当院では2008年8月からClinac21EXによる前立腺IMRTを開始し、2009年6月に施設基準が受理された。2010年2月にはNovalis Txによる前立腺IMRTを開始し、2012年6月からはVISICOILを使用した前立腺IMRTを開始した。 <目的> 画像誘導放射線治療(IGRT)が保険収載され、当院でもIGRTが可能なNovalis Txを用いてIMRTを行っている。IGRT を行うためには、位置照合装置(ExacTrac、OBI、CBCT)の精度管理が重要である。今回は前立腺IMRT(腹臥位、骨照合)の位置照合の流れと、位置照合装置の精度管理方法及び骨照合と前立腺照合の比較結果を報告する。 <方法> MV中心とレーザー照準器が一致している状態で、付属のファントムを用いて日々のExacTracとOBIのレーザー照準器に対する変位を測定した。次に、実際の治療時の骨照合でのsetup errorの値と、骨照合から前立腺で照合した時の差をinterfractional organ motionとして測定した。 <結果> ExacTracの中心誤差はLR0.22±0.08、AP-0.10±0.05、SI-0.21±0.08mm。OBIの中心誤差はガントリ角度0°、90°、180°、270°において1mm以内、CBCTの中心誤差はLR-0.09±0.21、AP0.39±0.21、SI-0.01±0.36mmであった。骨照合によるsetup errorはLR-0.04±0.27、AP-0.05±0.42、SI0.13±0.35mmであった。前立腺のinterfractional organ motionはLR-0.06±0.37、AP0.24±1.27、SI0.52±1.58mmであった。 <考察> レーザー照準器に対する位置照合装置(OBI、ExacTrac)の中心誤差は各々1mm以内で管理できており、セットアップマージンを縮小できる可能性があり、2種類の位置照合装置を管理し特徴を生かすことで、より精度の高い治療を短時間で行うことができると考えられる。 interfractional organ motionがある程度抑制できたのは、腹臥位によるシェル固定とExacTracにより骨照合での6軸のセットアップエラーを極力抑えた効果ではないかと考えられる。 <課題> 今後はintrafractional organ motionの評価も行い、適切なマージンを検討していきたい。また、VISICOILを使用することで確認ができた前立腺の呼吸性移動に対して、呼吸性移動が大きい場合にどのように対処するか考える必要がある。 |
|
| |
| 会員発表2 |
|---|
AAPM(54th Annual Meeting in Charlotte、USA)Best Paper in 2011 受賞報告 大垣市民病院 高木 等 会員 |
|
当然のことながら、迷惑メールであろうと思い、知り合いの先生方にも伺いましたが、まさか本当ではないであろうとの言う御意見でした。それで、AAPM事務局(Chief-Editor)へ問い合わせをしたところ、正真正銘のBest Paper in 2011受賞案内であることが判明しました。よって、急遽、米国ノースカロライナ州のシャーロット:Charlotte NC,USAにおいて開催される米国医学物理学会 (AAPM : The American Association of Physicists in Medicine)に参加することになり、AAPM会期中(2012 7/29-8/2)の7/30にCharlotte NC, USA Convention Centerで執り行われるCeremonyとReceptionに出席させて頂くこととなった次第です。学会発表を伴わずに、大手を振って、AAPMに参加させて頂けることは、医学物理士である私にとって、一度は参加したい国際的医学会であったこともあり、降って湧いたような話であり、極めて感慨深く幸せな事でした。 私の論文が掲載されたジャーナルは、JACMP(Journal of Applied Clinical Medical Physics)であり、先に述べた如く、AAPM配下のMedical Physicsと同様の放射線医学雑誌です。Medical Physics とJACMPでの2011年の掲載論文の中から選ばれ受賞したことになります。受賞に際しては、主筆者他、共同筆者すべてに表彰状が贈られ、副賞として小切手($500)を頂く事も出来ました。また、米国における学会授賞式典は、日本の学会での授賞式とは、大きく異なり、大きな学会主会場が満杯になり、立ち席がある程の学会関係者が各受賞者を皆でお祝いし、Ceremonyが、PM6:30から、1時間半、Receptionが1時間、その後もMusic ConcertがPM11:00まで続けられました。軽くドレスアップして参列した私と妻は、日本人がゼロに近いメインホールの最前列の受賞者特別席において、式典を十二分に満喫し、祝賀会を含め、貴重で一生忘れられない幸せで最高の思い出を作ることが出来ました。妻にも大きな助けをもらい、十分な理解の上で、好きな仕事と研究に没頭させてもらうことができ感謝しております。夫婦仲も極めて良好であり、結婚25年目の銀婚式にあたる年でもあり、妻への大きなプレゼントをすることもできました。 仕事や研究などに専念すると妻が・・・、と言う若い研究者の方々、ご安心あれ、その秘訣はありますよ。 近年、放射線治療の急激な発展に伴い、世界中の研究者が数多くの論文を投稿されており、アクセプトされるにも、かなりの先見性のある内容が必要であり、査読も非常に厳しく、しっかりとした英語論文が要求されます。放射線治療関連のジャーナルに掲載されるだけでも困難を極める大変熱い時代となっています。その中で、このようなAwardを受賞できたことは、身に余る光栄であると感じております。 ここで、米国医学物理学会の大要を紹介させて頂きます。全世界から、4000〜5000人の参加のある大規模な学会です。参加者は、世界中の医学物理士を中心として、放射線腫瘍医、放射線治療技師であり、発表演題数は、1000演題以上あります。主な演題としては、各種画像診断および放射線治療における物理学的評価や新しい装置の開発および様々な臨床的有用性の検討などです。日本からの参加者数は、毎年30〜50人程度です。参加者は東京大学、京都大学、名古屋大学、国立がんセンター、放射線総合医学研究所など国内主要大学および大規模医療施設にて、主に研究活動をしている理工系および保健学科出身の医学物理士です。現在、米国での医学物理士数は約5000人(放射線腫瘍医とほぼ同数)であり、米国での医学物理士は医者とほぼ同格での扱いであり、Ph Dの学位を取得した医学物理士が大いに活躍しています。米国の有名なAAPMへの有数参加施設としては、テキサス州にあるMDアンダーソンキャンサーセンター、オックスフォード大学、ハーバード大学、MIT(マサチューセッツ工科大学)等々があります。 ここで、受賞した掲載論文内容を簡潔に述べさせて頂きます。放射線治療装置の治療台上で、患者様のセットアップ状態をナビゲーションして、その体表面の変化をリアルタイムにモニタリングし、放射線照射中の体動および放射線治療期間中の体型変化を客観的なデータとして取得し判断することにより、放射線治療の照射精度管理をする新しい技術開発に関する研究論文です。昨今、画像誘導放射線治療:IGRT(Image Guided Radiotherapy)が注目されています。IGRTでカバーしきれない範囲を今回開発した技術が網羅することができたことが、世界中の研究者たちから評価された理由であると考えています。現在、Novalis Txに付設して、治療の際に使用しています。本論文の詳細は、寄稿した論文を一読下さい。 本研究がここまでの成果を上げる事ができたのは、研究の許可を出して頂いた山口前院長および曽根現院長を始めとする病院幹部の方々の御理解があってこそであります。大きな研究をするためには、病院内の理解と各種委員会の承諾を得られなくてはいけません。研究施設では、このような確立したシステムがあるとおもわれますが、自治体病院においては、決して十分であるとは思えません。この経緯を経験することもとても重要であったと考えます。前述したように病院内における最大のプロジェクトを遂行する課程で、多忙を極める中でも、すべてを完結することも必要でしょう。実務と学術(研究活動)の両立が必要不可欠です。私にとっては、このような状況下においても、大きな成果を得る事ができた理由として考えるのは、一重に、大垣市民病院の伝統的な学問に対する追求心と向上心の中で鍛えられた賜物であり、周囲の方々の深い御理解と御協力があってこそであると確信しております。海外学会へ参加するには、渡米・滞在費用および学会参加登録費(非会員の場合:AAPMでは、$1,520)が必要となります。大垣市民病院では、伝統的な背景より、従来より、国内学会は勿論の事、国際学会への発表においも、コメディカルスタッフに対して、7〜10割の各種費用を支出して頂けます。誠に有り難い事です。今回においては、発表はありませんでしたが、曽根現院長の御理解と御配慮により、出張扱い(10割支給)として頂けました。病院幹部の方々に心より深く感謝申し上げたいと思います。 ただし、目標とした学位を取得しても国際学会で受賞したとしても背景的には何も変わることはありません。ただ、変わることは自分自身に大きな責任が重くのしかかると言うことだと思われます。その責任とは、国際的な土俵に立った時にも日本のPh Dであると認められることです。その立場で、どのように国際的な活躍ができるかが勝負となるのでしょう。私は、あと8年現役を続けることができますので、その期間は、まだまだ先を見据えて前進したいと考えています。もう一つ、学位を取得して、大学での教育に携わる先生方も多くなって参りました。大学あるいは大学院での高等教育を受ける環境は、整ってきたと言うことになります。ところが、教育現場が第一線ではありません。あくまで、本当の意味での第一線は、現場である大学病院から始まり、国立、県立、市立、民間病院であると私は思っています。高等教育を受けて、修士や博士を取得して社会に出てくる学生たちの受け皿として、各々の病院が希望に満ちた環境を提供できるようにしていかなければいけないと考えています。よって、私は、大学院生を教育できるような環境整備に着手できるように体勢を強化していくつもりでいます。今年の春より、名古屋大学大学院生を教育・実習・バイトとしての雇入れをすることもできました。その大学院生が、来春は当院に就職してくれることにもなりました。私が、目指している目標が一つづつ実現できている気がします。ところが、彼らを生かすも殺すも病院の環境が左右します。彼らをしっかり指導できる人材の育成から始まり、彼らと共に将来を歩んでいく現スタッフらの理解、協調性、向上心などなど、すべてをランクアップする必要があるでしょう。どこかで辻褄が合わなくなると、妬み、やっかみなどの程度が大きくなり、環境がじわじわと悪化してしまいます。これでは、高等教育を受けてくる意味が薄れてしまいます。これらの発生を整理し、しっかりとした基盤から再構築して行くことを私の使命とし、邁進して行く所存であります。 【謝 辞】 最後に、名古屋大学医学部保健学科前教授 小幡康範先生の御指導の素晴らしさ、藤田保健衛生大学医学部教授 小林英敏先生に丁寧な御指導頂いた事、共同研究者の方々、現放射線治療スタッフである橋ノ口信一技師、藤原 宏技師、柳瀬豊子さん、小寺圭子さんにも御協力を頂いた事に深く感謝致します。また、橋ノ口技師も平成24年春の第68回日本放射線技術学会総会学術大会での発表に対して、銅賞を授かりました。我が放射線治療室は、今年、日米でのダブル受賞という名誉を得て、記憶に残る年となりました。本当に感激の限りです。 今回、平成22年に完成した新しい放射線治療室をも全世界にまで知らせる事が出来たことは大きな栄誉であります。大垣市民病院に勤務させて頂いて早30年になります。多くの経験や大きな試練をさせて頂いた事を糧にして、これからも素晴らしく、大好きな大垣市民病院のために最大限に尽力しつつ、技師会活動にも最大限の御協力をさせて頂きたいと思っております。 |
|
| |
| 特別講演 |
|---|
| サイバーナイフ ラジオサージェリーシステムのご紹介 日本アキュレイ株式会社 営業本部長 鈴木 敦 先生 |
||||||||||||||||
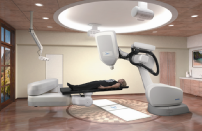
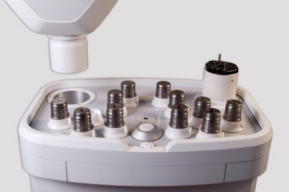
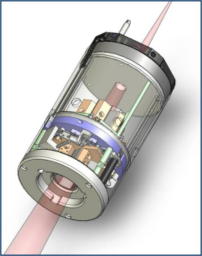
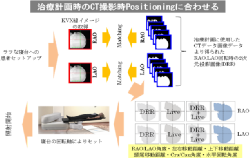
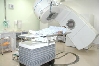
サイバーナイフシステムは、米国スタンフォード大学の脳外科医 J.アドラー教授が開発した放射線治療装置で、世界一号機は1994年に稼働を開始しました。本邦では1997年に一号機が稼働を開始し、2012年11月末現在27台が設置されています。頭頸部の定位放射線治療装置として開発されたサイバーナイフシステムですが、様々な改良を加えて現在では第四世代となり、体幹部へとその治療領域を広げています。 サイバーナイフは大きく2つの特長を有します。 第一は、6軸の回転軸を持つコンピュータ制御のロボットマニュピュレータに小型リニアックを搭載しているため、多方向からの照射が可能になり、正常組織や重要臓器に対する線量を出来得る限り低く抑えながら、腫瘍病巣に対しての線量集中が容易に行える点です。 第二は、治療部位・臓器の動きに対応するトラッキング機能です。サイバーナイフは、頭蓋内病変のように体動のみに影響を受ける照射部位、呼吸運動による周期的な動きのある部位あるいは前立腺のように必ずしも周期的な動きを呈さない部位というように、照射部位の動きの特徴に合わせてトラッキングをIntra-fractionに行います。 本稿では、これらの特長を説明します。 2. システムの構成 (図1) システムは主にロボットマニュピュレータ、直線加速器、患者寝台、X線管球、フラットパネルディテクタ、シンクロニーカメラ、治療計画装置(MultiPlan)で構成されています。
① ロボットマニュピュレータ
① 直線加速器
① 患者寝台
② X線管球・フラットパネルディテクタ
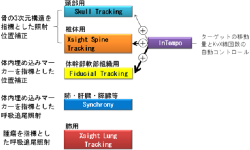
① Skull Tracking
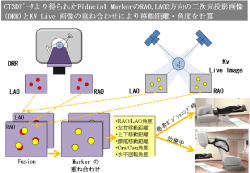
① Xsight Spine Tracking
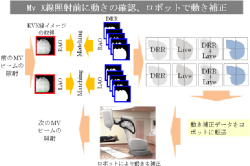
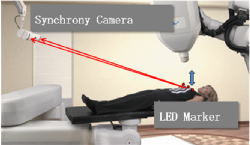
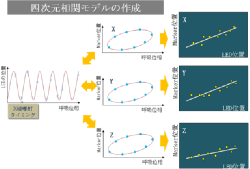
③ Synchrony
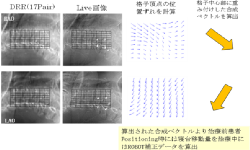
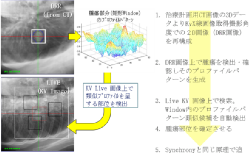
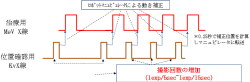
④ Xsight Lung Tracking
4. 最後に |
||||||||||||||||
| |
| 教育講演 |
|---|
| 標準計測法12の概要 名古屋大学大学院医学系研究科医療技術学専攻医用量子科学講座 准教授 小口 宏 先生 |
|
抄 録 |
|
| |